大量的研究已經表明金納米顆粒可以有效降低皮膚、肺、腸道的感染風險。在多種表面配體的幫助下,金納米材料表現出了高效抗菌活性和優異的生物相容性。尤其是金納米簇這一金納米材料,不僅抗菌性能優秀,還具有熒光特性,是一種能力強大的材料。
在另一方面,細菌纖維素(BC)具有高機械強度高、透光性、超軟度、水吸收性能強等特點,其多孔結構也與組織的細胞基質類似,非常適合作為敷料以加速皮膚的再生。更重要的是,高度透光的細菌纖維素薄膜能夠更加方便觀察敷料下傷口在愈合過程中的形貌變化。
因此,通過金納米簇和細菌纖維素的特點,南方科技大學微流控-生物材料實驗室設計了一種智能敷料,可在治療過程中自我檢測剩余納米藥物的濃度。研究將氨基苯硼酸(ABA)修飾的金納米簇(A-GNCs)裝載到細菌纖維素薄膜上形成抗菌傷口敷料,該敷料在治療多藥耐藥性細菌感染傷口時可通過原位比色法實時顯示剩余A-GNCs納米藥物的剩余量。A-GNCs可在紫外激發下發射明亮桔色熒光,而與此同時細菌纖維素薄膜在傷口處濕潤狀態下呈現透明的性質,因此BC- A-GNCs納米復合材料會隨著A-GNCs的釋放顯示桔色熒光強度逐漸降低的現象,從而為患者提供更換敷料的合適時間點。
相關工作以“Fluorescent and Antibacterial Aminobenzeneboronic Acid (ABA)-Modified Gold Nanoclusters for Self-Monitoring Residual Dosage and Smart Wound Care”為題發表在ACS Nano。
文章要點
一、A-GNCs的表征
對A-GNCs的表征顯示,其具有2納米左右的平均直徑且晶格結構清晰,在溶液中呈現亮黃色,而在365納米激發下發射高強度的桔色熒光(圖1)。A-GNCs具有優異的抗菌性能,SEM顯示A-GNCs能夠破壞細菌細胞壁造成融合,從而發揮強效的抗菌作用。

圖1 A-GNCs的基本表征
二、BC-A-GNCs納米復合薄膜
細菌纖維素具有良好的機械強度和巨大的比表面積,非常適合裝載A-GNCs形成敷料。實驗發現,當A-GNCs溶液濃度為32 μg/mL時,幾乎所有的A-GNCs都吸附在細菌纖維素薄膜上,驗證了細菌纖維素的高裝載容量。 隨著溶液濃度進一步增加,研究發現128 μg/mL的 A-GNCs溶液能夠導致最大化的裝載能力,因此作者選擇在這個濃度制備BC-A-GNCs納米復合材料(BGN)。對A-GNCs 在BGN里的釋放行為進行研究發現,由于部分A-GNCs存在于表面,突釋行為發生在最初的3天,而在5天后,A-GNCs的累計釋放量可達88%,展現了緩慢持續的釋放行為。經過7天的時間,剩余的A-GNCs濃度大概在12 μg/mL(而抗菌的最小抑制濃度MIC為8.75 μg/mL),表明BGN即將失去治療能力并且應當在該段時間內被更換(圖2)。
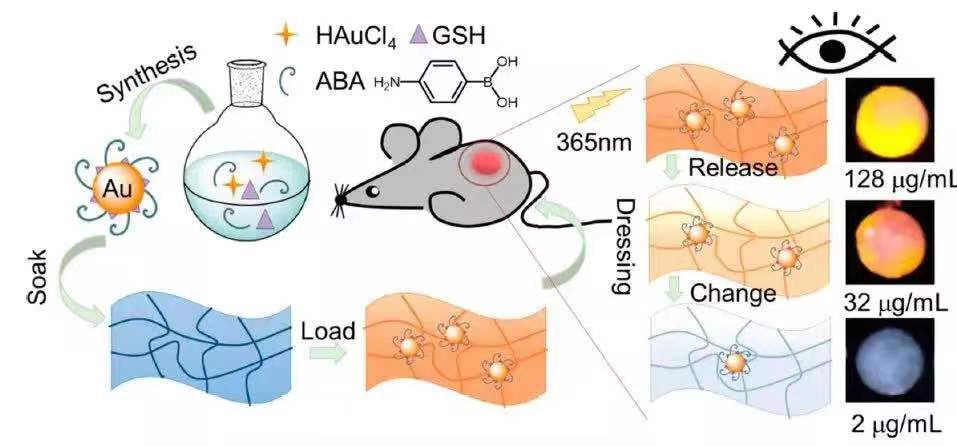
圖2 裝載A-GNCs的細菌纖維素支架示意圖
三、BC-A-GNCs納米復合薄膜的抗菌性能
隨后,作者研究了BGN的抗菌性能和生物相容性。研究發現,裝載了A-GNCs的BGN薄膜能夠抑制革蘭氏陰性菌及其相應耐藥菌株的增殖。在與革蘭氏陰性菌及其相應耐藥菌株接觸24小時后,BGN展現出了非常明顯的生長抑制區域。對細菌纖維素和BGN的血液生物相容性進行溶血分析可知,4小時的孵育不會對大鼠紅細胞產生任何溶血作用,證明BGN作為敷料可進行血液接觸應用。此外,將正常細胞放到BGN敷料上進行細胞活性檢測也進一步證實了BGN具有高度的生物安全性。
四、抗耐藥菌評估
最后,研究評價了BGN在革蘭氏陰性菌感染傷口模型中的治療作用。綠膿桿菌是慢性感染傷口中最常見的細菌,在治療14天后,研究發現綠膿桿菌感染傷口的愈合面積比例達到了91 ± 3.1%,而耐藥性綠膿桿菌感染傷口的愈合面積比例也達到了96 ± 2.5%,說明A-GNCs摻雜的細菌纖維素薄膜能夠加速感染傷口的愈合。 由于薄膜的透光性,作者可以在日光下直接觀察傷口愈合過程并定量分析剩余的A-GNCs濃度。隨著時間的推移,BGN可逐漸釋放A-GNCs,相應地敷料顏色變得更加暗淡,在第七天時,BGN就基本無法觀察了,這表明也BGN失去了治療能力并且應當被替換(圖6)。此外,對敷料下肉芽組織生長進行觀測也能夠非常準確的評價傷口愈合行為。而死的或未活化組織不僅能夠阻止傷口愈合過程,也會增加感染的風險。因此,通過BGN觀測傷口愈合可避免敷料的頻繁、不必要更換,從而減低二次傷害風險。
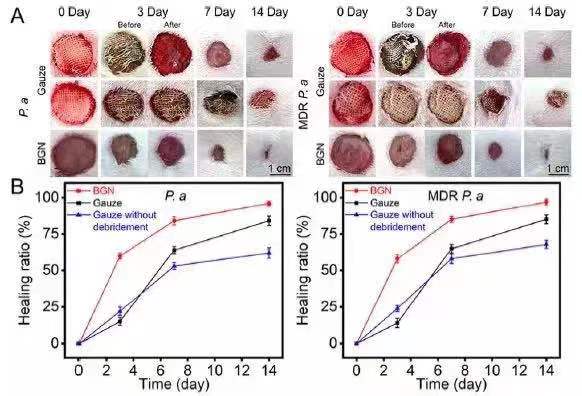
圖3 傷口愈合評價
?
結論
? ? ? ?為了可視化監測納米藥物傷口敷料,作者發展了一種新型策略,通過將納米藥物的熒光性能和支架材料的透光性相結合,可原位顯示敷料中剩余藥物量。在這一策略中,作者使用氨基苯硼酸改性的金納米簇作為具有強效抗菌性能的熒光納米藥物,同時選擇細菌纖維素薄膜作為透明支架材料。在傷口愈合過程中,A-GNCs的熒光強度隨著釋放行為的進行而逐漸降低,利用此現象可在納米藥物濃度低于最低抑菌濃度時及時更換敷料。因此,敷料狀態的實時監測只需簡單使用紫外光源就可以實現,而容易造成傷口破壞的敷料反復更換則可以被有效避免。
? ? ? ?文獻鏈接: https://pubs.acs.org/doi/10.1021/acsnano.1c06139